Ceimic

Is í an cheimic an disciplín eolaíoch a bhaineann le dúile agus comhdhúile comhdhéanta d’adamh, móilíní agus iain: a gcomhdhéanamh, a struchtúr, a n-airíonna, a n-iompar agus na hathruithe a dhéantar orthu le linn imoibrithe le substaintí eile.[1][2][3][4]
Faoi raon feidhme a ábhair, tá áit idirmheánach ag an gceimic idir an fhisic agus an bhitheolaíocht.[5] Uaireanta tugtar an eolaíocht lárnach uirthi toisc go leagann sí síos an bhunchloch chun na ndisciplíní eolaíochta bunúsacha agus feidhmiúla a thuiscint ar leibhéal bunúsach.[6] Mar shampla, míníonn an cheimic gnéithe de cheimic na bplandaí (luibheolaíocht), an chaoi a gcruthaítear carraigeacha igneacha (geolaíocht), an chaoi a ndéantar ózón atmaisféarach agus an chaoi a ndíghrádaíter truailleáin chomhshaoil (éiceolaíocht), airíonna na hithreach ar an ngealach (cosmaicheimic), conas a oibríonn cógais (cógaseolaíocht), agus conas fianaise Aigéad dí-ocsairibeanúicléasach (ADN) a bhailiú ag láthair choire (eolaíocht fhóiréinseach).
Pléann an cheimic ábhair mar an chaoi a n-idirghníomhaíonn adamh agus móilíní trí nasc ceimiceach chun comhdhúile ceimiceacha nua a ghiniúint. Tá dhá chineál nasc ceimiceach ann: 1. naisc cheimiceacha phríomhúla .i. naisc chomhfhiúsacha, ina roinneann adamh leictreon amháin nó níos mó; naisc ianacha, ina ndeonaíonn adamh leictreon amháin nó níos mó d’adamh eile chun ian (caitiain agus ainiain) a tháirgeadh; naisc mhiotalacha agus 2. naisc cheimiceacha tánaisteacha .i. naisc hidrigine; naisc d'fhórsa Van der Waals, idirghníomhaíocht ian-ian, idirghníomhaíocht ian-déphol srl.

Sanasaíocht
[cuir in eagar | athraigh foinse]Tagann an focal ceimic ó mhionathrú ar an bhfocal ailceimic, a thagair do shraith cleachtas níos luaithe a chuimsigh gnéithe den cheimic, den mhiotaleolaíocht, den fhealsúnacht, den astralaíocht, den réalteolaíocht, den mhisteachas agus den míochaine. Is minic a fheictear go bhfuil an ailceimic nasctha leis an tóraíocht chun mhiotail luaidhe nó eile a iompú ina n-ór, cé go raibh suim ag ailceimiceoirí i go leor cheisteanna na ceimice nua-aimseartha.[7] Faightear an focal nua-aimseartha ailceimic ón bhfocal Araibis الكیمیاء (al-kīmīā) B’fhéidir go bhfuil bunús na hÉigipte leis seo ós rud é go dtagann al-kīmīā ón nGréigis χημία (chimeía), a dhíorthaítear ar a seal ón bhfocal Kemet, arb é ainm ársa na hÉigipte sa teanga Éigipteach é. De rogha air sin, féadfaidh al-kīmīā teacht ó χημεία, rud a chiallaíonn "teilgthe le chéile".
Prionsabail nua-aimseartha
[cuir in eagar | athraigh foinse]
Is í samhail reatha an struchtúir adamhaigh ná samhail na meicnice candamaí. [8] Tosaíonn an cheimic thraidisiúnta le staidéar a dhéanamh ar bhuncháithníní, adaimh, móilíní,[9] comhdhúile, miotail, criostail agus comhbhailiúcháin de dhúile eile. Is féidir staidéar a dhéanamh ar dhúile i staideanna soladacha, leachtacha, gásacha agus plasmacha, ina n-aonar nó i dteannta a chéile. Is gnách go mbíonn na hidirghníomhaíochtaí, na himoibrithe agus na claochluithe a ndéantar staidéar orthu sa cheimic mar thoradh ar idirghníomhaíochtaí idir adaimh, rud a fhágann go ndéantar atheagrú ar na naisc cheimiceacha a choinníonn na hadaimh le chéile. Déantar staidéar ar iompraíochtaí den sórt sin i saotharlann cheimice.
Go steiréitipiciúil, úsáideann an tsaotharlann foirmeacha éagsúla d'earraí gloine saotharlainne faoi leith. Mar sin féin, níl earraí gloine lárnach sa cheimic, agus déantar cuid mhór den cheimic thurgnamhach (chomh maith le ceimic fheidhmeach/tionsclaíoch) gan earraí gloine.

Is éard is imoibriú ceimiceach ann ná athrú ina gclaochlaítear substaint ina substaint nua amháin nó níos mó.[10] Is é bunús a leithéid de chlaochlú ceimiceach ná atheagrú na leictreon sna naisc cheimiceacha idir adaimh. Is féidir é a léiriú go siombalach trí chothromóid cheimiceach, a mbíonn adaimh mar ábhair i gceist leis de ghnáth. Is ionann líon na n-adamh ar chlé agus ar dheis sa chothromóid le haghaidh claochlaithe cheimicigh. (Nuair a bhíonn líon na n-adamh ar gach taobh éagothrom, tugtar imoibriú núicléach nó meath radaighníomhach ar an gclaochlú.) Tá an cineál imoibriúcháin cheimicigh a d’fhéadfadh substaint a dhéanamh agus na hathruithe fuinnimh a d’fhéadfadh a bheith ag gabháil leis srianta ag rialacha bunúsacha áirithe, ar a dtugtar [[dlí ceimiceach|dlíthe ceimiceacha.
Bíonn cúinsí fuinnimh agus eantrópachta tábhachtach i gcónaí i mbeagnach gach staidéar ceimiceach. Déantar substaintí ceimiceacha a aicmiú i dtéarmaí a struchtúir, a gcéimeanna, chomh maith lena gcomhdhéanamh ceimiceacha. Is féidir anailís a dhéanamh orthu trí uirlisí anailíse ceimiceacha a úsáid, .i. speictreascópacht agus crómatagrafaíocht. Tugtar ceimiceoirí ar eolaithe atá i mbun taighde ceimiceach. Déanann mórchuid na gceimiceoirí speisialtóireacht i bhfo-dhisciplín amháin nó níos mó. Tá roinnt coincheap riachtanach chun staidéar a dhéanamh ar cheimic; seo cuid acu:
Damhna
[cuir in eagar | athraigh foinse]Sa cheimic, sainmhínítear damhna mar rud ar bith a bhfuil fosmhais agus toirt aige (tógann sé spás) agus atá comhdhéanta de cháithníní. Tá fosmhais ag na cáithníní a chuimsíonn damhna mais freisin- ní bhíonn fosmhais ag gach cáithnín, mar an fótón. Is féidir le damhna a bheith ina íon shubstaint cheimiceach nó ina mheascán de shubstaintí.[11]
Adamh
[cuir in eagar | athraigh foinse]
Ba é an Gréagach Democritos (t. 450 R. Ch.) a chéadchuir i bhfáth an teoraic go raibh na damhnaí uile déanta d'adaimh. De réir an fhealsaimh úd, ní féidir leanúint de roinnt damhna ar bith go síoraí, mar go dtiocfaí ar deireadh ar cháithníní nó mhionbhair den damhna nach bhféadfaí a roinnt níos mó. Ar cháithníní díobh sin, thug Democritos an t-ainm (Gréigis: άτομον, atmos (adamh), a chiallaíonn aonad do-roinnte. B'inmheasta dó go raibh na hadaimh an-mhion agus go raibh uimhir ollmhór díobh fiú sa ghiota ba lú de dhamhna a bhí sofheichte.
Go deimhin, bhí os cionn dhá mhíle bliain le himeacht sula bhfuarthas fianaise thurgnamhach go raibh dúile déanta de na haonais bhunúsacha úd.
I ngach adamh tá núicléas faoina lucht deimhneach i lár baill agus, mórthimpeall air sin, leictreoin (nó leictreon) le lucht diúltach.
Dúil cheimiceach
[cuir in eagar | athraigh foinse]Is éard is dúile ann ná substaintí nach féidir a dhianscaoileadh go ceimiceach ina substaintí eile níos simplí.
Tugtar substaintí íona ar shubstaintí nach meascáin iad. Is dúile nó comhdhúile iad substaintí íona.
Cuirtear na dúile seo taobh le taobh i dtábla a dtugtar an tábla peiriadach air.
Tá siombail ag gach dúil, mar shampla, H = hidrigin.
Ba é an t-eolaí Dmítrí Meindeiléiv a chuir an chéad bhun leis an tábla peiriadach seo sa bhliain 1869. Tá gach dúil atá ar eolas liostaithe i dtábla peiriadach na ndúl.
Comhdhúil
[cuir in eagar | athraigh foinse]Is éard is comhdhúil ann ná aon substaint cheimiceach a chruthaítear de thoradh imoibriú ceimiceach ina n-aontaítear dhá dhúil éagsúla, nó níos mó, de réir comhshuíomh seasta idir na dúile.
Nuair a dhéantar comhdhúil as a chuid dúl, bíonn airíonna difriúla de ghnáth ag an gcomhdhúil le hais airíonna na ndúl as a ndearnadh é. Mar shampla, is solad bán é clóiríd sóidiam (salann coitianta) atá réasúnta neamhimoibríoch go ceimiceach. Is iad na dúile as a bhfuil sé déanta ná sóidiam, miotal airgid atá an-imoibríoch, agus clóirín, gás glas atá an-imoibríoch.
I gcomhdhúil cheimiceach, bíonn adaimh na ndúl éagsúil ceangailte lena chéile le naisc cheimiceacha—ianacha nó chomhfhiúsacha.
Cuirtear coibhneas na ndúl agus struchtúr inmheánach na comhdhúile in iúl le foirmlí éagsúla ceimiceacha. Is comhdhúil an t-uisce ina mbíonn hidrigin agus ocsigin i gcóimheas 2:1.
Tá an t-adamh ocsigin idir an dá adamh hidrigine, agus uillinn 104.45° eatarthu.

Mar shampla, tugann an fhoirmle seo a leanas d'uisce (H2O) le fios dúinn go bhfuil uisce ina chomhdhúil agus go bhfuil dhá adamh hidrigine nasctha d'aon adamh ocsaigine amháin.
Níl comhdhúile liostaithe i dtábla peiriadach na ndúl.
Móilín
[cuir in eagar | athraigh foinse]
Is éard is móilín ann ná an chuid is lú de dhúil nó de chomhdhúil is féidir a bheith ann go neamhspleách.
Tugtar ceimic mhóilíneach nó fisic mhóilíneach ar na heolaíochtaí a bhaineann leis an ábhar seo, ag brath ar chlaonadh an fhócais.
Substaint agus meascán
[cuir in eagar | athraigh foinse]Is cineál damhna é substaint cheimiceach le comhdhéanamh cinnte agus tacar d'airíonna.[12] Tugtar meascán de bhailiúchán substaintí. Samplaí de mheascáin is ea aer agus cóimhiotail.[13]
Mól agus méid na substainte
[cuir in eagar | athraigh foinse]Is éard is mól nógram-mhóilín ar mheáchan admhach den dúil sin ina ghraim. Cuir i gcás, is ias 1.008g. 14.008g. 16.000g. 35.46g 126.9 g agus 238 g na gram-adaimh se na dúile hidrigib, nítrigin, ocsaigin, clóirín iaidín agus úráiniam ar leith.[14]
Pas
[cuir in eagar | athraigh foinse]An 4 phas nó staid ar féidir go mbeidh damhna iontu: solad, leacht, gás agus plasma. Braitheann pas damhna ar leith ar an teocht is an brú atá i bhfeidhm air. Tugtar an pastrasdul ar an athrú ó phas amháin go pas eile, cosúil le fiuchadh nó leá. Léiríonn pasléaráid pasanna damhna ag teochtaí is brúnna éagsúla,
Chomh maith leis na hairíonna ceimiceacha ar leith a dhéanann idirdhealú idir aicmithe ceimiceacha éagsúla, is féidir ceimiceáin a bheith ann i roinnt céimeanna. Den chuid is mó, tá na haicmithe ceimiceacha neamhspleách ar na haicmithe bulcphassana seo; áfach, tá roinnt pasanna níos coimhthíocha neamh-chomhoiriúnach le hairíonna ceimiceacha áirithe. Is éard atá i bpas ná sraith staideanna de chóras ceimiceach a bhfuil mór-airíonna struchtúracha comhchosúla acu, thar raon coinníollacha, amhail brú nó teocht.
Is gnách go dtagann airíonna fisiciúla, mar shampla dlús agus innéacs athraonta faoi luachanna atá sainiúil don phas. Sainmhínítear pas dhamhna leis an phas-trasdul, is é sin nuair a théann fuinneamh a chuirtear isteach sa chóras nó a thógtar amach chun struchtúr an chórais a atheagrú, in ionad na mórchoinníollacha a athrú.
Uaireanta is féidir an t-idirdhealú idir pasannaa bheith leanúnach in ionad teorainn scoite a bheith acu, sa chás seo meastar go bhfuil an t-ábhar i staid fhorchriticiúil. Nuair a thagann trí staid le chéile bunaithe ar na coinníollacha, tugtar an tríphointe air agus ós rud é go bhfuil sé seo do-athraitheach, is bealach áisiúil é chun sraith coinníollacha a shainiú.
Taispeánann a lán substaintí pasanna soladacha iomadúla. Mar shampla, tá trí phas d’iarann soladach (alfa, gáma, agus deilte) a athraíonn bunaithe ar theocht agus brú. Príomhdhifríocht idir pasanna soladacha is ea criostalstruchtúr, nó socrú, na n-adamh. Paseile a bhíonn coitianta i staidéar na ceimice ná an pas leachtach, is é sin staid na substaintí atá tuaslagtha i dtuaslagán uiscí (is é sin, in uisce).
I measc na bpasanna nach bhfuil chomh heolach tá plasmaí, comhdhlútháin Bhose-Einstein agus comhdhlútháin fheirmíónacha agus na pasanna paramaighnéadacha agus fearómaighnéadacha d'ábhair mhaighnéadacha. Cé go ndéileálann na pasanna is eolaí le córais tríthoiseacha, is féidir analógacha a shainiú i gcórais déthoiseacha, ar tugadh aird orthu maidir lena ábharthacht do chórais sa bhitheolaíocht.
Nascadh
[cuir in eagar | athraigh foinse]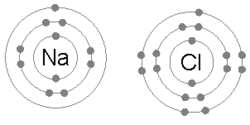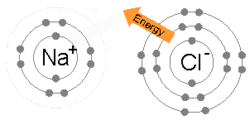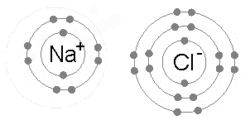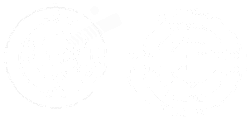
Na fórsaí leictreacha a cheanglaíonn adaimh i móilíní agus pais sholadacha neamh-mhóilíneacha. In aon adamh, timpeallaíonn na leictreoin an núicléas i bhfithiseáin i sceallaí timpeall an núicléis. Muna mbíonn an sceall seachtrach lán le leictreoin, an uasmhéid atá ceadaithe don adamh sin, bíonn an t-adamh éagobhsaí agus fonn air nasc a dhéanamh le hadamh eile. Aithnítear 3 shaghas naisc phríomhúil. An nasc ianach, mar atá i gclóiríd sóidiam, NaCl (salann mín), inar chaill an sóidiam leictreon agus ar ghnóthaigh an clóirín leictreon, ionas go gcoinnítear na hiain seo le chéile trí aomadh frithpháirteach idir Na+ is Cl-. Sa nasc comhfhiúsach, mar atá i gclóirín, Cl2, bíonn cuid de na leictreoin bainteach leis an dá núicléas. Nuair a nascann dhá adamh hidrigine (H) le hadamh amháin ocsaigine (O), cruthaítear móilín uisce, H2O, agus bíonn dhá nasc chomhfhiúsacha ann. Sa nasc miotalach, mar atá i sóidiam, Na, bíonn na fiúsleictreoin dílogánaithe agus bainteach le cuid mhaith núicléas, rud a thugann seoltacht leictreach don mhiotal. Tugtar nasc singil ar nasc comhfhiúsach ina bhfuil dhá leictreon i gceist, nasc dúbailte ar cheann le 4 leictreon, agus nasc triarach ar cheann le 6 leictreon. Comharthaítear na naisc seo i bhfoirmlí ceimiceacha le -, =, is ≡. Tugtar an nascfhuinneamh ar an bhfuinneamh is gá chun nasc ceimiceach a bhriseadh (mar shampla, chun móilín clóirín, Cl2, a athrú in dhá adamh clóirín, 2 Cl).
Fuinneamh
[cuir in eagar | athraigh foinse]Is cumas chun obair a dhéanamh é an fuinneamh, de réir na fisice de. Is iomaí cineál fuinnimh ann. Is fuinneamh cinéiteach é an fuinneamh atá i réad de bharr a ghluaisne. Is fuinneamh poitéinsiúil domhantarraingthe é fuinneamh atá i réad de bharr a airde os cionn plána tagartha, mar shampla, cloch os cionn na talún. Is fuinneamh meicnice é an dá shaghas fuinnimh sin curtha le chéile, fuinneamh cinéiteach is fuinneamh poitéinsiúil. Is cineál fuinnimh eile é an teas. Nuair a dóitear breosla, mar shampla peitreal, fuasclaítear fuinneamh ceimiceach an bhreosla ina theas.
De réir bhunchoincheapanna na fisice, ní féidir fuinneamh a chruthú ná a dhíothú ach is féidir é a athrú ó chineál amháin fuinnimh go cineál eile. Tarlaíonn a leithéid in inneall ar bith, mar shampla in inneall dócháin inmheánaigh.
Imoibriú ceimiceach
[cuir in eagar | athraigh foinse]I gcás dó damhna A in aer (nó in ocsaigin) deirtear gur imroibrigh an damhna sin le hocsaigin chun damhna nua (éagsúil leo siúd araon) a ghiniúint. Ach is féidir le damhna airithe oimibriú le damhna eile (seachas ocsaigin) freisin chun damhna nó damhnaí eile a ghiniúimnt mar an gcéanna. De ghnáth trí fhuinneamh a ídiú nó a ghnóthú ag an gcóras. Tugtar oimibriú ceimiceach ar imoibrithe dá leithéid siúd ina ngintear damhna nua amháin, nó níos mó ná damhna amháin, ó imoibriú idir dhá dhamhna eile, agus tugtar athraithe ceimiceacha ar na hathraithe bunúsacha a tharla de thoradh na n-oibrithe. viz.:
- amhna A + damhna B imoibriú ceimiceach -> damhna C
Iain agus salainn
[cuir in eagar | athraigh foinse]Is éard is ian ann ná adamh nó móilín a bhfuil lucht leictreach aige. Má dhéanann adamh nó móilín leictreon dá chuid a thabhairt uaidh, nó leictreon de chuid adaimh nó móilín eile a ghlacadh chuige, ní bheidh sé neodrach a thuilleadh. Beidh lucht leictreach aige—lucht diúltach, má fuair sé leictreon ar iasacht, lucht deimhneach, má thug sé ceann uaidh. Is dual don dá chineál lucht leictreach an cineál céanna a éaradh (a ruaigeadh uaidh) agus an cineál eile a aomadh (a tharraingt chuige). Ina lán comhdhúl ceimiceach, tá an dá chineál ian ann, agus iad curtha in aice a chéile sa chriostal ionas go bhfuil gach ian timpeallaithe ag iain den chineál eile. Mar sin, coinníonn an fórsa aomtha—an nasc ianach an criostal le chéile.
Bíonn na comhdhúile ianacha sothuaslagtha san uisce, toisc gur tuaslagóir polach é an t-uisce. Is é sin, tá pol diúltach agus pol deimhneach ag an móilín uisce - deirtear gur déphol é an móilín uiscec—é go bhfuil an móilín féin neodrach. Aomann an pol diúltach iain dheimhneacha, agus na hiain dhiúltacha ag tarraingt ar an bpol eile.
Sampla de chomhdhúil ianach é an gnáthshalann, is é sin, an chlóiríd sóidiam. Tá an salann an-difriúil leis an dá dhúil a bhfuil sé comhdhéanta as, mar atá, an clóirín agus an sóidiam. Gás buíghlas nó uaine é an clóirín a bhfuil boladh láidir as, agus nimh atá ann don duine, nó oibríonn sé go tubaisteach ar na scamhóga: níl tiúchan mór clóirín san aer análaithe de dhíth le héidéime scamhógach a tharraingt ar an duine, is é sin, na scamhóga a líonadh le sreabh nó leacht a thachtfaidh an t-othar (sin é an tuige, dála an scéil, gur baineadh úsáid as an gclóirín mar ghás cogaidh—arm ceimiceach—sa Chéad Chogadh Domhanda). Maidir leis an sóidiam, is miotal alcaileach é—is é sin, miotal bog atá chomh haraiciseach chun imoibriú a dhéanamh le substaintí eile is go rachaidh sé trí thine san uisce. Má chuirtear clóirín agus sóidiam in aice le chéile, imoibreoidh siad le chéile go fiáin fíochmhar le salann a dhéanamh. Tabharfaidh gach adamh sóidiam aon leictreon amháin ar iasacht do cheann de na hadaimh chlóirín, ionas go gcruthófar iain chlóiríde, Cl-, agus iain sóidiam, Na+.
Aigéadacht agus bunatacht
[cuir in eagar | athraigh foinse]Is minic gur féidir substaint a aicmiú mar aigéad nó mar bhun. Tá roinnt teoiricí éagsúla ann a mhíníonn iompraíocht aigéid-bhuin. Is é an ceann is simplí na teoiric Arrhenius, a deir gur aigéad í conhdhúil ar bith a thugann na hiain hiodróiniam (H3O+) i dtuaslagáin agus is bun í aon chomhdhúil a thugann iain hiodrocsaíde (OH−) i ndobharthuaslagáin. De réir theoiric Brønsted–Lowry is aigéad é an speiceas a bhfuil claonadh ann chun prótón hidrigine (H+) a chailliúint agus is bun é an speiceas a bhfuil claonadh ann chun prótón a ghlacadh.
Tríú teoiric choitianta is ea teoiric Leictreonach Lewis faoi aigéid agus buanna, atá bunaithe ar naisc cheimiceacha nua a dhéanamh. Míníonn teoiric Lewis gur aigéad é speiceas ar bith a ghlacann le dís leictreon agus is bun é speiceas ar bith a ghlacann le dís leictreon. De réir na teoirice seo, is iad na rudaí is tábhachtaí atá á malartú ná na luchtanna.[15][16] Tá bealaí éagsúla ann inar féidir substaint a aicmiú mar aigéad nó mar bhun, mar is léir i stair an choincheapa seo.[17]
Déantar neart aigéid a thomhas go coitianta trí dhá mhodh. Tomhas amháin, bunaithe ar shainmhíniú Arrhenius ar aigéadacht, is ea pH, ar tomhas é ar thiúchan iain hidriginiam i dtuaslagán, mar a chuirtear in iúl é ar scála logartamach diúltach. Mar sin, tá tiúchan ard iain hidriginiam ag tuaslagáin a bhfuil pH íseal acu agus is féidir a rá go bhfuil siad níos aigéadach. Tomhas eile atá bunaithe ar shainmhíniú Bhrønsted-Lowry is ea an tairiseach díthiomsúcháin aigéid (Ka), a thomhaiseann cumas coibhneasta substainte gníomhú mar aigéad faoin sainmhíniú Bhrønsted-Lowry ar aigéad. Is é sin, is dóichí go dtabharfaidh substaintí a bhfuil Ka níos airde acu iain hidrigine in imoibrithe ceimiceacha ná iad siúd a bhfuil luachanna Ka níos ísle acu.
Ocsdí
[cuir in eagar | athraigh foinse]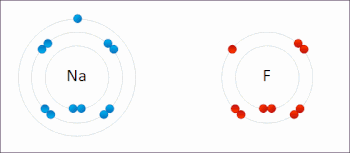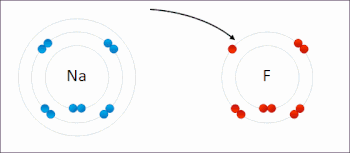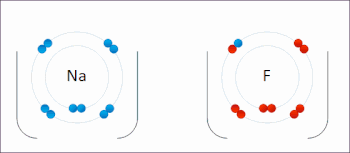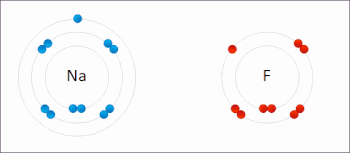
Is cineál imoibrithe cheimicigh é ocsdí ina bhfuil staideanna ocsaídiúcháin na n-adamh aithrithe. Tá sé mar chomhartha sóirt ag imoibrithe ocsdí aistriú iarbhír nó foirmiúil leictreon idir speicis cheimiceacha, go minic le speiceas amháin (an dí-ocsaídeoir) ag dul faoi ocsaídiú (leictreoin a chailleadh) le linn do speiceas eile (an t-ocsaídeoir) ag dí-ocsaídiú (gnóthachain leictreon).[18] Deirtear gur ocsaídíodh an speiceas ceimiceach as a mbaintear an leictreon, agus deirtear gur dí-ocsaídíodh an speiceas ceimiceach a gcuirtear an leictreon leis. I bhfocail eile:
Cothromaíocht cheimiceach
[cuir in eagar | athraigh foinse]In imoibriú ceimiceach, is éard is cothromaíocht cheimiceach ná an riocht nó an staid ina bhfuil na himoibreáin agus na táirgí araon i láthair i dtiúchan nach bhfuil aon chlaonadh eile iontu athrú le hama, ionas nach mbeidh aon athrú inbhraite ar airíonna an chórais.[19] Tarlaíonn an staid seo nuair a théann an tulimoibriú ar aghaidh ag an ráta céanna leis an cúlimoibriú. De ghnáth ní bhíonn rátaí imoibrithe na dtulimoibrithe agus na gcúlimoibrithe ina nialas, ach cothrom. Mar sin, níl aon glanathruithe i dtiúchan na n-imoibreán agus na dtáirgí. Tugtar cothromaíocht dhinimiciúil ar staid den sórt sin[20]
Dlíthe ceimiceacha
[cuir in eagar | athraigh foinse]Cinntíodh ó thurgnaimh a rinne Robert Boyle (1627–1691), Antoine-Laurent de Lavoisier agus John Dalton le linn an seachtú agus an t-ochtú aois déag go raibh damhnaí rialaithe ag dlíthe áirithe.
Rialaítear imoibrithe ceimiceacha le dlíthe áirithe, ar coincheapa bunúsacha iad sa cheimic anois. Seo a leanas cuid acu:
- Dlí Avogadro
- Dlí Beer-Lambert
- Dlí Boyle (1662, a bhaineann le brú agus toirt)
- Dlí Charles (1787, a bhaineann le toirt agus teocht)
- Dlíthe Fick
- Dlí Gay-Lussac (1809, a bhaineann le brú agus teocht)
- Prionsabal Le Chatalier
- Dlí Henry
- Dlí Hess
- Dlí Imchoimeád na Maise
- Dlí imchoimeád an fhuinnimh
- Dlí an chomhshuímh thairisigh
- Dlí na gcomhréir iolrach
- Dlí Raoult

Stair na Ceimice
[cuir in eagar | athraigh foinse]Is deacair a rá cathain a thosaigh stair na ceimice dáiríre. I measc na gceimiceoirí is luaithe, is féidir na mná Bablónacha a bhí ag driogadh cumhrán a lua. I bhfad roimhe sin, áfach, fuair na daoine amach go raibh ábhair áirithe indóite agus ábhair eile dodhóite. Fórsa rúndiamhair ab ea an tine, a bhí in ann ábhar a chlaochlú go hábhar eile, rud ba dhúspéis leis na daoine. Ba í an tine a chabhraigh leis an duine iarann nó gloine a dhéanamh an chéad uair riamh. Nuair a d'éirigh sé coitianta dearcadh ar an ór mar mhiotal luachmhar, chuir na daoine suim san ailceimic. Is é is ailceimic ann ná na hiarrachtaí a rinneadh leis an ór a dhéanamh go sintéiseach, gan é a bhaint as an talamh. Ní raibh i gceist leis an ailceimic go fóill ach réamheolaíocht nó próta-eolaíocht, ach mar sin féin, d'fhoghlaim agus d'fhorbair na hailceimiceoirí modhanna oibre a chuaigh chun tairbhe na bhfíorcheimiceoirí i ndiaidh thréimhse na hailceimice.
D'aimsigh na hailceimiceoirí go leor próiseas ceimiceach, rud a chuidigh le forbairt na ceimice nua-aimseartha. I gcaitheamh na staire, thréig na hailceimiceoirí ab fhearr an rúndiamhracht agus na piseoga a bhí ag roinnt leis an ailceimic, agus iad ag fáil eolais ar fhíornádúr an damhna, ionas gur tháinig dearcadh ní b'eolaíochtúla chucu dá n-ainneoin. I measc rogha na n-ailceimiceoirí, is fiú Geber, nó Abu Musa Jabir ibn Hayyan, agus Paracelsus, nó Philippus Theophrastus Aureolus Bombastus von Hohenheim, a lua. Ba é Robert Boyle, áfach, a d'oscail an geata ón ailceimic go dtí an cheimic. Léiriú maith ar a dhearcadh is ea teideal an tsaothair ba thábhachtaí dár scríobh sé, mar atá, The Skeptical Chymist, is é sin, An tAilceimiceoir Sceiptiúil. Mar sin féin, bhí an Baoilleach ina ailceimiceoir i gcónaí. Ba é Antoine Laurent Lavoisier an chéad cheimiceoir nua-aimseartha, ámh. B'eisean a leag amach Dlí Imchoimeádta na Maise sa bhliain 1783, agus b'eisean ba thúisce a tháinig ar an tuiscint cheart ar an dóchán mar phróiseas ceimiceach. Roimh a lá féin, chreid na heolaithe gurbh ionann an dóchán agus an breosla a bheith ag tabhairt uaidh "flógastón", dearcadh a bhí bunaithe, ar bhealach, ar an míthuiscint sheanársa gur cineál damhna nó dúile atá sa teas. Thaispeáin Lavoisier nach amhlaidh a bhí, ach gurbh é an rud a bhíonn ag titim amach le linn an dócháin ná go bhfuil an breosla ag cumasc leis an ocsaigin.
Ceann de na dúile ceimiceacha ab ea an ocsaigin, agus thóg sé na blianta fada ar na heolaithe na dúile go léir a aithint, a aonrú, a ainmniú agus a aicmiú. Ba mhór an cuidiú san obair seo an tuiscint a tháinig chuig Dmitrí Meindeiléiv, John Newlands, agus Lothar Meyer timpeall na bliana 1870—is é sin, nuair a ordaíodh na dúile ceimiceacha de réir a meáchan adamhach, go raibh na saintréithe céanna á nochtadh go tráthrialta. D'oibrigh Meindiléiv amach an chéad tábla peiriadach, agus na dúile curtha taobh le chéile de réir a meáchan adamhach agus na saintréithe comhchosúla. Ó bhí an tábla seo mantach in áiteanna, bhí Meindiléiv ábalta tuairim a thabhairt i dtaobh na ndúl a bhí ag fanacht lena bhfionnachtain i gcónaí. Nuair a aonraíodh an chéad uair iad, fíoraíodh a chuid tairngreachtaí.
Cleachtadh
[cuir in eagar | athraigh foinse]Fodhisciplíní
[cuir in eagar | athraigh foinse]- An Cheimic Neamhorgánach: déanann an fodhisciplín seo taighde ar na comhdhúile neamhorgánacha, is é sin, na comhdhúile nach bhfuil slabhraí d'adaimh an charbóin iontu.
- An Cheimic Orgánach: Fadó, b'ionann an cheimic orgánach agus an bhithcheimic. Sa lá atá inniu ann, áfach, tugtar ceimic orgánach ar cheimic na gcomhdhúl carbónacha. Tá an carbón in ann slabhraí móra fada a dhéanamh nach bhfuil teorainn ná críoch leo, agus an dúrud de chomhdhúile éagsúla ann a bhfuil slabhraí den chineál sin iontu. is ábhar taighde ann féin, mar sin, na slabhraí seo agus na struchtúir éagsúla mhóilíneacha a gcuireann siad bun leo.
- An Bhithcheimic: Sin é an t-ainm a thugtar sa lá atá inniu ann ar cheimic na neacha beo agus ar an dóigh a n-úsáidtear coincheapa agus modhanna oibre na ceimice sa bhitheolaíocht.
- An Cheimic Fhisiceach: Shoiléirigh an mheicnic chandamach sa bhliain 1926, go raibh bunús fisice taobh thiar den cheimic. Go bunúsach, déanann an ceimiceoir fisiceach taighde ar an mbaint atá ag an gceimic leis an bhfisic. Mar shampla, is suim leis teirmidinimic na ceimice, cinéitic na n-imoibrithe ceimiceacha, an leictriceimic, an mheicnic staitisteach, agus an speictreascópacht. Is deacair an cheimic fhisiceach a aithint go soiléir ón bhfisic mhóilíneach. Tá gá ag an gceimiceoir fisiceach leis an gcalcalas agus é ag fréamhú a chuid cothromóidí. Baineann an cheimic fhisiceach go dlúth leis an gceimic theoiriciúil agus le ceimic an chandaim.
- An Cheimic Theoiriciúil: Is éard atá i gceist leis an gceimic theoiriciúil ná réasúnaíocht theoiriciúil na fisice agus na matamaitice a chuirtear i bhfeidhm ar cheisteanna na ceimice. Go háirithe, tugtar ceimic chandamach ar an dóigh a bhfeidhmítear an fhisic chandamach sa cheimic. Sna blianta i ndiaidh an Dara Cogadh Domhanda, chuaigh na ríomhairí an oiread sin i bhfeabhas gur féidir a rá go bhfuil a leithéid de bhrainse ann agus ceimic ríomhaireachta, is é sin, forbairt agus feidhmiú na ríomhchlár le freastal ar shainriachtanais na ceimice. Tá dlúthbhaint ag an gceimic theoiriciúil le fisic an damhna chomhdhlúite agus leis an bhfisic mhóilíneach. Níl i gceist go bunúsach leis an gceimic theoiriciúil ach fisic, ar an gcaoi chéanna nach bhfuil sa bhitheolaiocht theoiriciúil ach ceimic agus fisic.
- Is í an cheimic núicléach an brainse den cheimic a phléann leis an radaighníomhaíocht: an úsáid a bhaintear as an radaighníomhaíocht le taighde a dhéanamh ar ghnáth-imoibrithe ceimiceacha (radaiceimic), an tionchar atá ag mais na n-iseatóp éagsúil ar na himoibrithe ceimiceacha (ceimic iseatópach), agus speictreascópacht an athshondais mhaighnéadaigh núicléigh—is é sin, brainse speictreascópachta a théann i dtuilleamaí saintréithe maighnéadacha na núicléas le móilíní a aithint. Is féidir "ceimic núicléach" a thabhairt ar an dóigh a n-úsáideann fisiceoirí núicléacha modhanna oibre nó coincheapa na ceimice le taighde a dhéanamh ar eamhnú agus ar chomhleá na núicléas.
Brainsí eile de chuid na ceimice is ea: an réaltcheimic, an cheimic atmaisféarach, an innealtóireacht cheimiceach, an fhaisnéisíocht cheimiceach, an leictriceimic, ceimic an chomhshaoil, an cheimic shreabhach, an gheocheimic, an cheimic ghlas, stair na ceimice, eolaíocht na n-ábhar, ceimic na míochaine, an bhitheolaíocht mhóilíneach, an nanaitheicneolaíocht, an cheimic orgánaimhiotalach, an pheitriceimic, an chógaseolaíocht, an fhótaiceimic, an fhíticeimic, an cheimic pholaiméarach, an cheimic soladstaide, an tsonaiceimic, an cheimic fhormhóilíneach, an cheimic dhromchlach, agus an teirmiceimic.
Tionscal
[cuir in eagar | athraigh foinse]Léiríonn an tionscal ceimiceach gníomhaíocht eacnamaíoch thábhachtach ar fud an domhain. Sa bhliain 2013, bhí díolacháin de US $980.5 billiún ag na 50 táirgeoir ceimiceach is fearr ar domhan, le corrlach brabúis de 10.3%.[21]
Cumainn ghairmiúla
[cuir in eagar | athraigh foinse]- Société Française de Chimie (SFC)
- American Chemical Society
- American Society for Neurochemistry
- Institut de chemie du Canada
- Sociedad Química del Perú
- International Union of Pure and Applied Chemistry
- Royal Australian Chemical Institute
- Koninklijke Nederlandse Chemische Vereniging[nasc briste go buan]
- Royal Society of Chemistry
- Society of Chemical Industry
- World Association of Theoretical and Computational Chemists
An Cheimic Idirphearsanta
[cuir in eagar | athraigh foinse]Sanasaíocht
[cuir in eagar | athraigh foinse]- Ailceimic na hÉigipte [5,000 BC – 400 BC], Leabharlann Chathair Alastair
- Ailceimic na Gréige [332 BC – 642 AD], na Greigigh i réim i gCathair Alastair
- Ailceimic na nArabach [642 AD – 1200], na hArabaigh i réim i gCathair Alastair, e.g. Is é Jabir an príomh-cheimiceoir.
- Ailceimic na hEorpa [1300 – Inniu], Gerber a thóg ar Cheimic na nArabach
- Ceimic [1661], Boyle The Sceptical Chemist
- Ceimic [1787], Lavoisier Élémentaire de Chimie
- Ceimic [1803], Dalton Atomic Theory
Féach freisin
[cuir in eagar | athraigh foinse]- Fillteán Eolaíochta TS COGG http://www.cogg.ie/wp-content/uploads/ceimic-filltean-eolaiochta-ts.pdf
- CICLIPÉID EILE – ANOTHER UNFINISHED SCIENCE ENCYCLOPAEDIA IN IRISH, https://irishforenglishspeakers.blog/2017/04/10/ciclipeid-eile-another-unfinished-science-encyclopaedia-in-irish/ Curtha i gcartlann 2017-04-30 ar an Wayback Machine
- Ceimiceoir agus Liosta ceimiceoirí
- Tábla peiriadach
- Liosta dúl de réir ainm
- (fr) Actualités Chimie, sur le site Futura-Sciences.com
- (fr) La chimie au lycée, sur le site du CNRS Curtha i gcartlann 2006-12-06 ar an Wayback Machine
- (en) Eric Weisstein's world of chemistry
- (fr) Vidéos participatives sur la chimie pour les élèves du secondaire
Leitheoireacht sa bhreis
[cuir in eagar | athraigh foinse]- Ceimic na hArdteistiméireachta Ghnáthleibhéal & Ardleibhéal. Fírici Fillte. An Chomhairle um Oideachais Gaeltachta & Gaelscolaíochta. The Celtic Press.
- Atkins, P.W. Galileo's Finger (Oxford University Press)
- Chang, Raymond. Chemistry 6th ed. Boston: James M. Smith, 1998. ISBN 0-07-115221-0.
- MacCann, Diarmuid . Ceimic. An Chláir Nua don Mheánteistiméireacht. An Gúm 1985.
- Hussey, Matt. Nod don Eolach, Gasaitéar Eolaíochta.An Gúm 1999
- Kennedy, Porter, Scott. Eolaíocht Bhunúsach. An Gúm 1990.
- Pauling, L. The Nature of the chemical bond (Cornell University Press) ISBN 0-8014-0333-2
- Pauling, L., and Wilson, E. B. Introduction to Quantum Mechanics with Applications to Chemistry (Dover Publications) ISBN 0-486-64871-0
- Pauling, L. General Chemistry (Dover Publications) ISBN 0-486-65622-5
Liosta léitheoireachta do mhicléinn ollscoile
[cuir in eagar | athraigh foinse]- Atkins,P.W. Physical Chemistry (Oxford University Press) ISBN 0-19-879285-9
- Atkins,P.W. et al. Molecular Quantum Mechanics (Oxford University Press)
- Ó Cinnéide, Seán. Ceimic Bhunúsach 1. An Chéad Chló, Rialtas na hÉireann.
- McWeeny, R. Coulson's Valence (Oxford Science Publications) ISBN 0-19-855144-4
- Stephenson, G. Mathematical Methods for Science Students (Longman)ISBN 0-582-44416-0
- Smart and Moore Solid State Chemistry: An Introduction (Chapman and Hall) ISBN 0-412-40040-5
- Atkins,P.W., Overton,T., Rourke,J., Weller,M. and Armstrong,F. Shriver and Atkins inorganic chemistry (4th edition) 2006 (Oxford University Press) ISBN 0-19-926463-5
- Clayden,J., Greeves,N., Warren,S., Wothers,P. Organic Chemistry 2000 (Oxford University Press) ISBN 0-19-850346-6
- Voet and Voet Biochemistry (Wiley) ISBN 0-471-58651-X
Naisc Sheachtracha
[cuir in eagar | athraigh foinse]- Dréacht den Ardteistiméireacht Sonraíocht na Ceimice
- National 5, Chemistry.
- MIT OpenCourseWare | Chemistry
- EuroChem (European Portal for Chemistry - Database of Hazard Compounds, European Legislation) Curtha i gcartlann 2019-06-13 ar an Wayback Machine
- Chemistry Information Database
- Chemistry Research
- International Union of Pure and Applied Chemistry Curtha i gcartlann 2007-10-31 ar an Wayback Machine
- IUPAC Nomenclature Home Page, see especially the "Gold Book" containing definitions of standard chemical terms
- Material safety data sheets for a variety of chemicals Curtha i gcartlann 2007-10-16 ar an Wayback Machine
- Cook/Douglass Multimedia Achives Curtha i gcartlann 2006-10-22 ar an Wayback Machine contains videos of General Chemistry tutorials; worked out example problems
- BestChoice Stage 1 University Chemistry tutorial[nasc briste go buan] from University of Auckland
Tagairtí
[cuir in eagar | athraigh foinse]- ↑ "What is Chemistry?". Cartlannaíodh an bunleathanach ar 3 Deireadh Fómhair 2018. Dáta rochtana: 13 Márta 2021.
- ↑ "Definition of CHEMISTRY" (en).
- ↑ "Definition of chemistry | Dictionary.com" (en).
- ↑ "Chemistry Is Everywhere".
- ↑ Carsten Reinhardt. Chemical Sciences in the 20th Century: Bridging Boundaries. Wiley-VCH, 2001. ISBN 3-527-30271-9. pp. 1–2.
- ↑ Theodore L. Brown, H. Eugene Lemay, Bruce Edward Bursten, H. Lemay. Chemistry: The Central Science. Prentice Hall; 8 edition (1999). ISBN 0-13-010310-1. pp. 3–4.
- ↑ "History of Alchemy". Cartlannaíodh an bunleathanach ar 8 Meitheamh 2011. Dáta rochtana: 13 Márta 2021.
- ↑ "chemical bonding". Britannica. Encyclopædia Britannica. Aisghafa 1 November 2012.
- ↑ Matter: Atoms from Democritus to Dalton Curtha i gcartlann 2007-02-28 ar an Wayback Machine by Anthony Carpi, Ph.D.
- ↑ IUPAC Gold Book Definition Curtha i gcartlann 4 Márta 2007 ar an Wayback Machine
- ↑ Armstrong, James (2012). "{{{title}}}". Brooks/Cole.
- ↑ "{{{title}}}" (2005). Upper Saddle River, New Jersey: Pearson Prentice Hall.
- ↑ "{{{title}}}" . ASM International.
- ↑ Ceimic Bhunúsach 1. An Gram-adamh. Lth.85
- ↑ "The Lewis Acid-Base Concept". Apsidium. Cartlannaíodh an bunleathanach ar 27 Bealtaine 2008. Dáta rochtana: 18 Márta 2021.Teimpléad:Unreliable source?
- ↑ "History of Acidity".
- ↑ "History of Acidity".
- ↑ Tá ort na shonrú' 'teideal = agus' 'url = nuair a úsáideann {{ lua idirlín}}."". Cartlannaíodh an bunleathanach ar 2012-05-30.
- ↑ Atkins' Physical Chemistry.https://archive.org/details/atkinsphysicalch00pwat
- ↑ Atkins, Peter W.; Jones, Loretta (2008). Chemical Principles: The Quest for Insight (2nd ed.). ISBN 978-0-7167-9903-0.
- ↑ C&EN's Global Top 50 Chemical Firms For 2014. https://cen.acs.org/articles/92/i30/CENs-Global-Top-50-Chemical.html
