Amóinia
 | |
| Substaint cheimiceach | aicme eintiteas ceimiceach |
|---|---|
| Mais mhóilíneach | 17.026549096 Da |
| Ainmnithe in ómós | Séas Amón |
| Fionnachtaí nó aireagóir | Joseph Priestley |
| Tacsón ina n-aimsítear é | |
| Ról | príomh-mheitibilít |
| Struchtúr ceimiceach | |
| Foirmle cheimiceach | NH₃ |
 | |
| SMILES canónta | |
| InChI | Model 3D |
| Airí | |
| Dlús | 0.7625 kg/m³ (a 0 °C, gás) |
| Luas forleata fuaime | 415 m/s (0 °C, gás) |
| PKa | 9.21 |
| Tuaslagthacht | 34 g/100 g (uisce, 20 °C) |
| Móimint leictreach dhépholach | 1.471 D |
| Pointe leáite | −77.74 °C −78 °C |
| Fiuchphointe | −33.4 °C −33 °C (a 760 Torr) −33.33 °C (a 101.325 kPa) |
| Eantrópach mólarach caighdeánach | 192.5 J/(mol K) |
| Móimint leictreach dhépholach | 1.471 D |
| Eantalpacht chaighdeánach an fhoirmithe | −45.94 kJ/mol |
| Galbhrú | 8.5 atm (a 20 °C) |
| Guais | |
| Teorainn inlasta íochtair | 15 vol% |
| Teorainn inlasta uachtarach | 28 vol% |
| Dáileog mharfach íosta | 5,000 ppm (duine, mamach, ionanálú, 5 min) 1,500 mg/m³ (duine, ionanálú, 30 min) 5,000 ppm (mamach, ionanálú, 5 min) 3,317 ppm (luch saotharlainne, ionanálú, 1 h) 132 mg/kg (duine) |
| Dáileog mharfach airmheánach | 7 g/m³ (cat, coinín, ionanálú, 1 h) 4,600 mg/m³ (luch saotharlainne, ionanálú, 2 h) 4,500 ppm (luch saotharlainne, ionanálú, 1 h) 4,230 ppm (luch saotharlainne, ionanálú, 1 h) 21,430 ppm (luch saotharlainne, ionanálú, 30 min) 7 g/m³ (coinín, ionanálú, 1 h) 18,600 mg/m³ (francach saotharlainne, ionanálú, 5 min) 7,040 mg/m³ (francach saotharlainne, ionanálú, 30 min) 2,000 ppm (francach saotharlainne, ionanálú, 4 h) 17,401 ppm (francach saotharlainne, ionanálú, 15 min) 9,500 ppm (francach saotharlainne, ionanálú, 1 h) 40,300 ppm (francach saotharlainne, ionanálú, 10 min) 28,595 ppm (francach saotharlainne, ionanálú, 20 min) 20,300 ppm (francach saotharlainne, ionanálú, 40 min) 11,590 ppm (francach saotharlainne, ionanálú, 1 h) 7,338 ppm (francach saotharlainne, ionanálú, 1 h) 4,837 ppm (luch saotharlainne, ionanálú, 1 h) 9,859 ppm (coinín, cat, ionanálú, 1 h) 2,000 ppm (francach saotharlainne, ionanálú, 1 h) |
| Teocht uathadhainte | 651 °C |
| Meánteorainn nochta ualaithe ama | 18 mg/m³ (10 h, luach ar iarraidh) 35 mg/m³ (8 h, Stáit Aontaithe Mheiriceá) 25 ppm (, an Éigipt, an Astráil, an India, an tSeapáin, an Chóiré Theas, Meicsiceo, an Nua-Shéalainn, an Iorua, Peiriú, an tSualainn, an Tuirc, an Ríocht Aontaithe) 20 ppm (, an Ostair, an Bheilg, an Danmhairg, an Fhionlainn, an Ghearmáin, an Íoslainn) 14 mg/m³ (, an Coimisiún Eorpach, an Ungáir, an Ísiltír) 10 ppm (, an Fhrainc) 20 mg/m³ (, an Pholainn) 50 ppm (, an Téalainn, na hOileáin Fhilipíneacha) |
| Short-term exposure limit (en) | 27 mg/m³ (an Pholainn) 35 ppm (an Astráil, an India, an Chóiré Theas, Meicsiceo, an Nua-Shéalainn, Peiriú) 50 ppm (an Bheilg, an Fhionlainn, an Íoslainn, an tSualainn) 36 mg/m³ (an Coimisiún Eorpach, an Ungáir) 20 ppm (an Fhrainc) 20 mg/m³ (an Rúis) |
| Láithreach contúirteach don bheatha nó sláinte | 210 mg/m³ agus 300 ppm |
| Global warming potential (en) | 0 |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |
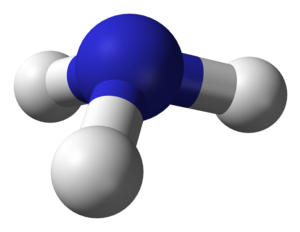
Is í an amóinia an ceann is tábhachtaí de chomhdhúile dénártha na hidrigine is na nítrigine. Is í a foirmle cheimiceach ná NH3 (móilín pirimidiúil, le nascuillinneacha timpeall 107°, bun lag. Bíonn pH timpeall 9.5 ag a tuaslagáin atá páirtneodraithe le haigéid láidre)[1]. Is gás í le teocht an tseomra faoi ghnáthbhrú an atmaisféir.
Is furasta an amóinia a aithint ar a boladh bréan sainiúil.
Nuair a thuaslagfar amóinia san uisce, gheofar tuaslagán bunata atá in ann aigéid a neodrú. Is é an t-ian amóiniam NH4+ is toradh d'imoibriú na hamóinia is an uisce, agus é á iompar sna comhdhúile mar a bheadh ian miotail ann. Mar sin, is féidir salainn éagsúla amóiniam a chruthú agus iad an-chosúil le salainn mhiotail. Samplaí de seo iad an chlóiríd amóiniam agus an níotráit amóiniam.
Úsáidtear an chlóiríd amóiniam mar spíosra - cuirtear le liocras í le blas níos géire a thabhairt dó. Maidir leis an níotráit amóiniam, is leasú talún agus ábhar pléasctha í.
Is nimh é an gás amóinia a oibríonn go dona ar na scamhóga, ach san am chéanna, is amhábhar tábhachtach í don tionsclaíocht.
Bíonn an amóinia ar fáil go nádúrtha i mún an duine agus na n-ainmhithe, go háirithe má fhágtar an mún sin ag iompú, agus mar sin, is féidir le seanfhual na n-ainmhithe feirme an dúlra a thruailliú go dona.
Is í an amóinia an pointe tosaigh dá lán craobhacha den tionsclaíocht cheimiceach.

Stair
[cuir in eagar | athraigh foinse]Chruthaigh Claude Louis BerthoIIet gur comhdhúil hidrígine is nítrigine í amóinia.
Bhí sé an-deacair an nasc idir an dá adamh i móilín na nítrigine N2 a bhriseadh leis an nítrigin sin a cheapadh i gcomhdhúile ceimiceacha.
Sa bhliain 1904, thosaigh an ceimiceoir Fritz Haber sa Ghearmáin ag forbairt an phróisis a thabhaigh clú agus cáil dó, is é sin, déantús na hamóinia. D'éirigh leis nítrigin an atmaisféir a chlaochlú go hamóinia sa tsaotharlann.
Sa bhliain 1909, d'éirigh le Haber agus Carl Bosch an próiseas seo a fhorbairt is a fhoirfiú—"modh oibre Haber agus Bosch", nó Haber-Bosch-Verfahren mar a deir an Ghearmáinis.
Bhí an t-aireagán seo chomh tábhachtach is gur thuill sé Duais Nobel na Ceimice do Haber.
Féach freisin
[cuir in eagar | athraigh foinse]- Is iomaí caint a tharraing saol Fritz Haber.
- amóiniam nó NH4
Tagairtí
[cuir in eagar | athraigh foinse]- ↑ Hussey, Matt (2011). "Fréamh an Eolais".
Naisc sheachtracha
[cuir in eagar | athraigh foinse]- International Chemical Safety Card 0414 (anhydrous ammonia)
- International Chemical Safety Card 0215 (aqueous solutions)
- National Pollutant Inventory - Ammonia
- Emergency Response to Ammonia Fertilizer Releases (Spills) for the Minnesota Department of Agriculture
- National Institute for Occupational Safety and Health - Ammonia Page

