Leibhéal fuinnimh

Ní féidir le córas meicniúil candamach nó cáithnín atá nasctha - is é sin, atá sáinnithe go spásúil - ach luachanna scoite fuinnimh áirithe, ar a dtugtar leibhéil fhuinnimh, a ghlacadh. Tá sé seo i gcodarsnacht le cáithníní clasaiceacha, ar féidir leo méid ar bith fuinnimh a bheith acu. Úsáidtear an téarma go coitianta le haghaidh leibhéil fuinnimh na leictreon in adaimh, iain, nó móilíní, atá nasctha ag réimse leictreach an núicléas, ach is féidir leo tagairt a dhéanamh freisin do na leibhéil fhuinnimh sa núicléas nó do na leibhéil rothlacha nó creathúla fuinnimh i móilíní. Deirtear go mbíonn an speictream fuinnimh i gcórais a bhfuil na leibhéil fhuinnimh scoite sin aige a chainníochtú. Deirtear go ndéantar speictream fuinnimh córais a bhfuil na leibhéil fhuinnimh scoite sin aige candamaithe.
Sa cheimic agus san fhisic adamhach, féadtar smaoineamh ar leictreonsceall, nó príomhleibhéal fuinnimh, mar fhithis leictreon amháin nó níos mó timpeall núicléas an adaimh. De réir theoiric Bhohr, bhí fithisí áirithe thart ar an núicléas, agus fad a bhí an leictreon in aon fhithis díobh sin, níor astaigh sé fuinneamh ar bith. Tugtar an "sceall 1" ar an sceall is gaire don núicléas (ar a dtugtar "sceall K " freisin), agus tar éis sin, tugtar an "sceall 2" (nó an "sceall L" ), ansin an "sceall 3" (nó "sceall M") , agus mar sin de, níos faide agus níos faide ón núicléas. Comhfhreagraíonn na scealla leis na príomh-chandamuimhreacha (n = 1, 2, 3, 4 ...), nó tá siad lipéadaithe in ord aibítre le litreacha a úsáidtear sa nodaireacht x-ghathach (K, L, M, N…).
Ní féidir ach líon seasta leictreon a bheith i ngach sceall: Is féidir leis an gcéad sceall suas le dhá leictreon a shealbhú, is féidir leis an dara sceall suas le hocht (2 + 6) leictreon a shealbhú, is féidir leis an tríú sceall suas le 18 (2 + 6 + 10) a choinneáil agus mar sin de. Is í an fhoirmle ghinearálta gur féidir leis an naoú sceall suas le 2(n2) leictreon a choinneáil. Ós rud é go n-aomtar leictreoin go dtí an núicléas, is gnách nach n-áitíonn leictreoin adaimh scealla seachtracha má tá na scealla istigh líonta go hiomlán cheana féin ag leictreoin eile. Mar sin féin, ní riachtanas docht é seo: d’fhéadfadh go mbeadh dhá nó fiú trí sceall seachtrach neamhiomlán ag adamh. (Féach riail Madelung le haghaidh tuilleadh sonraí.) Le haghaidh míniú ar an bhfáth go bhfuil leictreoin sna scealla seo féach cumraíocht na leictreon.[1]
Má tá an fuinneamh poitéinsiúil socraithe go nialas ag fad éigríochta ón núicléas adamhach nó ón móilín, an gnáthchoinbhinsiún, ansin tá fuinneamh féideartha diúltach ag staid nasctha leictreon.
Má tá adamh, ian, nó móilín ag an leibhéal fuinnimh is ísle is féidir, deirtear go bhfuil sé féin agus a leictreoin sa bhunstaid. Má tá sé ar leibhéal fuinnimh níos airde, deirtear go bhfuil sé flosctha, nó go bhfuil aon leictreon a bhfuil fuinneamh níos airde acu ná an bhunstaid flosctha. Má tá níos mó ná staid mheicniúil chandamach amháin ag an bhfuinneamh céanna, tá na leibhéil fhuinnimh “díchineálach”. Tugtar leibhéil fhuinnimh dhíchineálacha orthu ansin.
Míniú[cuir in eagar | athraigh foinse]
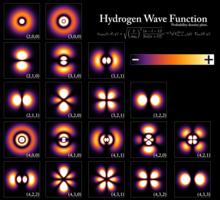
Eascraíonn leibhéil chandamaithe fuinnimh ón ngaol idir fuinneamh an cháithnín agus a thonnfhad. Maidir le cáithnín gaibhnithe mar leictreon in adamh, tá foirm na toinne seasta ag an tonnfheidhm.[2] Ní féidir ach staideanna cónaitheacha le fuinneamh a fhreagraíonn do shlánuimhreacha tonnfhaid a bheith ann; i gcás staideanna eile cuireann na tonnta trasna ar bhealach neamhdhearfach, agus mar thoradh air sin bíonn dlús dóchúlachta nialasacha. Samplaí bunúsacha a thaispeánann go matamaiticiúil conas a thagann leibhéil fuinnimh i gcrích is ea an cáithnín i mbosca agus an t-ascaltóir armónach candamach.
Stair[cuir in eagar | athraigh foinse]
Ba é an chéad fhianaise ar chainníochtú in adaimh ná an bhreathnóireacht, le Joseph von Fraunhofer agus William Hyde Wollaston, ar línte speictrim i solas na gréine go luath sna 1800idí. Mhol fisiceoir na Danmhairge Niels Bohr coincheap na leibhéal fuinnimh sa bhliain 1913 i teoiric Bohr den adaimh. Chuir Erwin Schrödinger agus Werner Heisenberg an teoiric mheicniúil chandamach nua-aimseartha, a thugann míniú ar na leibhéil fhuinnimh seo, i dtéarmaí na cothromóid Schrödinger chun cinn i 1926.
Adaimh[cuir in eagar | athraigh foinse]
Leibhéil fhuinnimh intreacha[cuir in eagar | athraigh foinse]
Sna foirmlí le haghaidh fuinneamh leictreon ag leibhéil éagsúla a thugtar thíos in adamh, socraítear an pointe nialasach le haghaidh fuinnimh nuair a fhágann an leictreon atá i gceist an t-adamh go hiomlán, .i. nuair a bhíonn príomhuimhir chandamach an leictreon n = ∞. Nuair a bhíonn an leictreon nasctha leis an adamh in aon luach níos dlúithe de n , tá fuinneamh an leictreon níos ísle agus meastar go bhfuil sé diúltach.
Leibhéal fuinnimh na staide fithisí: adamh/ian le núicléas + leictreon amháin[cuir in eagar | athraigh foinse]
Glac leis go bhfuil leictreon amháin i bhfithiseán adamhach tugtha in adamh (ian) atá cosúil le hidrigin. Déantar fuinneamh a staide a chinneadh go príomha trí idirghníomhaíochta leictreastataí leictreon (diúltach) leis an núicléas (dearfach). Tugtar leibhéil fhuinnimh leictreon timpeall núicléas le:
(idir 1 eV agus 103 eV, de ghnáth), áit a bhfuil R∞ mar tairiseach Rydberg, is í Z an uimhir adamhach, is í n an phríomhuimhir chandamach, is í h tairiseach Planck, agus c luas an tsolais. Maidir le hadaimh (iain) atá cosúil le hidrigin amháin, braitheann leibhéil Rydberg ar an bpríomhuimhir chandamach n.
Faightear an chothromóid seo trí fhoirmle Rydberg d'aon dúile cosúil le hidrigin (a thaispeántar thíos) a chomhcheangal le E = hv = hc/λ, ag glacadh leis gurb í an phríomhuimhir chandamach n thuas =n1 i bhfoirmle Rydberg agus n2 = ∞ (príomhuimhir chandamach den leibhéal fuinnimh as a shíolraíonn an leictreon, nuair a astaíonn sé fótón). Díorthaíodh foirmle Rydberg ó shonraí astaíochtaí speictreascópacha eimpíreacha.
Is féidir foirmle choibhéiseach a dhíorthú go meicniúil ó chothromóid Schrödinger, atá neamhspleách ó thaobh ama, le hoibreoir fuinneamh cinéiteach Hamilton a úsáideann tonnfheidhm mar dhualfheidhm chun na leibhéil fuinnimh a fháil mar luachanna dualfheidhme, ach bheadh tairisigh fhisiceacha eile curtha in ionad tairisigh Rydberg.
Idirghníomhaíochtaí leictreon-leictreon in adaimh[cuir in eagar | athraigh foinse]
Má tá níos mó ná leictreon amháin timpeall an adaimh, ardaíonn idirghníomhaíochtaí leictreon-leictreon an leibhéal fuinnimh. Is minic a dhéantar faillí de na hidirghníomhaíochtaí seo má tá forluí spásúil de thonnfheidhmeanna an leictreoin íseal.
Maidir le hadaimh il-leictreon, bíonn idirghníomhaíochtaí idir leictreoin ina gcúis nach bhfuil an chothromóid roimhe seo cruinn a thuilleadh mar a luaitear go díreach le Z mar an uimhir adamhach. Bealach simplí (cé nach bhfuil sé iomlán) chun é seo a thuiscint is ea mar éifeacht dhíonta, nuair a fheiceann na leictreoin sheachtracha núicléas éifeachtach de lucht laghdaithe, ós rud é go bhfuil na leictreoin laistigh nasctha go docht leis an núicléas agus go gcuireann siad a lucht ar ceal go páirteach. Mar thoradh air seo, déantar leasú garbh nuair a chuirtear lucht núicléach éifeachtach a shiombailítear mar Zeff atá ag brath go mór ar an bpríomhuimhir chandamach, in ionad Z.
I gcásanna den sórt sin, bíonn tionchar ag na cineálacha fithiseán (arna gcinneadh ag an chandamuimhir asamatach ℓ) chomh maith lena gcuid leibhéal laistigh d'éifeacht mhóilíneach Zeff, agus dá bhrí sin bíonn tionchar acu freisin ar leibhéil éagsúla fuinnimh leictreon adamhach. Cuireann prionsabal Aufbau, maidir le hadamh a líonadh le leictreoin le haghaidh cumraíochta leictreon, na leibhéil éagsúla fuinnimh seo san áireamh. Le haghaidh adaimh a líonadh le leictreoin sa bhunstaid, líontar na leibhéil fhuinnimh is ísle ar dtús agus tá siad ag teacht le prionsabal eisiaimh Pauli, prionsabal Aufbau, agus riail Hund.
Móilíní[cuir in eagar | athraigh foinse]
Cruthaítear naisc cheimiceacha idir adaimh an mhóilín toisc go ndéanann siad an staid níos cobhsaí do na hadaimh atá i gceist, rud a chiallaíonn go ginearálta go bhfuil suim na leibhéal fuinnimh de na hadaimh lena mbaineann sa mhóilín níos ísle ná mura mbeadh na hadaimh nasctha amhlaidh. De réir mar a théann adaimh ar leithligh i dteagmháil lena chéile chun nasc comhfhiúsach a dhéanamh, bíonn tionchar ag a bhfithiseáin ar leibhéil fhuinnimh a chéile, chun fithiseán móilíneach nascach agus neamh-nascach a fhoirmiú. Tá leibhéal fuinnimh na bhfithiseán nascach níos ísle, agus tá leibhéal fuinnimh na bhfithiseán neamh-nascach níos airde. Ionas go mbeidh an nasc sa mhóilín cobhsaí, lonnaíonn na leictreoin nascacha chomhfhiúsacha san bhfithiseán nascach fuinnimh is ísle, a fhéadfaidh a bheith léirithe ag siombailí mar σ nó π ag brath ar an staid. Is féidir fithiseáin chomhfhreagracha neamh-nascacha a léiriú trí réiltín a chur leo chun fithiseán σ * nó π * a thaispeáint. Is fithiseán neamh-nascach i móilín é fithiseán le leictreoin i scealla seachtracha nach nglacann páirt i nascadh agus tá a leibhéal fuinnimh mar an gcéanna le leibhéal an adaimh chomhdhéanaimh. Is féidir fithiseáin den sórt sin a léiriú mar n-fhithiseáin. De ghnáth is péirí aonair iad na leictreoin i bhfithiseán. I móilíní poladamhacha, bíonn leibhéil éagsúla fuinnimh chreathúil agus rothlaigh i gceist freisin.
Go garbh, is staid fuinnimh mhóilíneach í, .i. dualstaid den Hamaltún-mhóilíneach, suim na gcomhábhar leictreonach, creathúil, rothlach, núicléacha agus aistritheach, sa chaoi:
- E = E leictreonach +Ecreathúil + Erothlach + E núicléacha + E aistritheach
i gcás gur dual-luach é an E leictreonach den Hamaltún-mhóilíneach (luach an fhuinnimh phoitéinsiúil dromchla) ag geoiméadracht chothromaíochta an mhóilín. Tá na leibhéil fuinnimh mhóilíneacha lipéadaithe ag siombailí na dtéarmaí móilíneacha. Athraíonn sainfhuinnimh na gcomhpháirteanna seo de réir staid an shainfhuinnimh agus na substainte.
Léaráidí leibhéal fuinnimh[cuir in eagar | athraigh foinse]
Tá cineálacha éagsúla léaráidí leibhéal fuinnimh ann do naisc idir adaimh i móilín.
- Samplaí
Léaráidí na bhfithiseán móilíneach, léaráidí Jablonski, agus léaráidí Franck-Condon.
Trasdulta leibhéal fuinnimh[cuir in eagar | athraigh foinse]


Is féidir le leictreoin in adaimh agus i móilíní leibhéil fuinnimh a athrú (trasdulta a dhéanamh iontu) trí fhótón (de radaíocht leictreamaighnéadach) a astú nó a ionsú, a gcaithfidh a fhuinneamh a bheith comhionann go díreach leis an difríocht fuinnimh idir an dá leibhéal.
Tagairt[cuir in eagar | athraigh foinse]
- ↑ Electron Subshells. Corrosion Source. Retrieved on 1 December 2011.
- ↑ "Physics for Scientists and Engineers, 5th Ed." (2004) 2: 1129. W. H. Freeman and Co..



