Fiús (ceimic)
Sa cheimic, is éard is fiús dúile ann ná an oiread nasc ceimiceach is féidir le hadamh amháin a dhéanamh le hadaimh is móilíní eile. Tomhas is ea é, ar chumas nasctha adaimh nó dúile, sé sin, an méid adamh ar féidir leis cuingriú leo nó cá mhéad leictreon a chaithfidh sé gnóthú, cailleadh nó roinnt chun struchtúr triathgháis a bhaint amach.
Cur síos
[cuir in eagar | athraigh foinse]Cinntear cumas nasctha adaimh ar leith, de réir líon na n-adamh hidrigine a chuingríonn sé le. I meatán, tá fiús de 4 ag carbón; in amóinia, tá fiús de 3 ag nítrigin; in uisce, tá fiús de 2 ag ocsaigin; agus i gclóiríd hidrigine, tá fiús de 1 ag clóirín. Is féidir clóirín, toisc go bhfuil fiús de 1 aige, a chur in ionad hidrigine. Tá fiús de 5 ag fosfar i bpeinteaclóiríd fhosfair, PCl55. Léiríonn léaráidí fiúsanna de chomhdhúil cumas nasctha na ndúl, le línte tarraingthe idir dhá ghné, ar a dtugtar bannaí uaireanta, a léiríonn gaireacht sáithithe do gach dhúil. Taispeánann an dá thábla thíos roinnt samplaí de chomhdhúile éagsúla, a gcuid léaráidí fiúsanna, agus na fiúsanna do gach dúil den chomhdhúil.
| Comhdhúil | H2 Hidrigin |
CH4 Meatán |
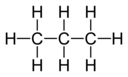
C3H8 Própán |
C2H2 Aicéitiléin |
|---|---|---|---|---|
| Léaráid | 
|
|
||
| Fiúsanna |
Hidrigin: 1 |
Carbón: 4 Hidrigin: 1 |
Carbón: 4 Hidrigin: 1 |
Carbón: 4 Hidrigin: 1 |
| Comhdhúil | NH3 Amóinia |
NaCN Ciainíd sóidiam |
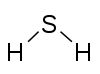
H2S Suilfíd hidrigine |
H2SO4 Aigéad sulfarach |
Cl2O7 Heaptocsaíd déchlóiríd |
XeO4 Tatrocsaíd xeanóIn | ||
|---|---|---|---|---|---|---|---|---|
| Léaráid | 
|
|

|

|

| |||
| Fiúsanna |
Nítrigin: 3 Hidrigin: 1 |
Sóidiam: 1 Carbón: 4 Nítrigin: 3 |
Sulfar: 2 Hidrigin: 1 |
Sulfar: 6 Ocsaigin: 2 Hidrigin: 1 |
Clóirín: 7 Ocsaigin: 2 |
Xeanón:8 Ocsaigin:2 }} Tagairtí[cuir in eagar | athraigh foinse]
|
