Hidrigin
 | |
| Substaint cheimiceach | dúil cheimiceach |
|---|---|
| Hidrigin sa tábla peiriadach | |
| Siombail cheimiceach | H |
| Uimhir adamhach | 1 |
| Mais adamhach | 1.008 |
| Cumraíocht leictreon | 1s¹ |
| Peiriad, Grúpa | peiriad 1 grúpa 1 uisce |
| Airíonna fisiceacha | |
| Dath | éadathach |
| Dlús | 0.08987 kg/m⁻³ |
| Leáphointe | −259.14 |
| Fiuchphointe | −252.87 |
| Comhéifeacht athraonta | 1.000132 |
| Leictridhiúltacht | 2.2 |
| Ga ianach | 54 |
| Leathré | luach ar iarraidh |
| Stair | |
| Aimsitheoir | Henry Cavendish, Mikhail Vassilyevich Lomonosov agus Antoine Lavoisier |
| Fionnachtain | 1766 |
| Eapainm | uisce |
 | |
Dúil cheimiceach neamh-mhiotalach is ea an hidrigin (Laidin: hydrogenium, ó Ghréigis: hydro: uisce, genes: ag cumadh, ag gineadh, ag cruthú). Is í an hidrigin an dúil is éadroime amuigh, is é "H" an tsiombail atá aici, agus is é a haon (1) an uimhir adamhach atá aici. Tá sí ina gás leis an ngnáth-theocht. Ó tá sí chomh héadrom, bhítí á húsáid sna héadromáin, ach ós rud é go bhfuil sí iontach so-adhainte, is iomaí timpiste a tharraing sí.
Níl dath sa hidrigin ná boladh aisti.
Iseatóip[cuir in eagar | athraigh foinse]
Níl ach aon phrótón amháin sa núicléas ag an ngnáth-hidrigin, nó an próitiam. Ach, tá dhá iseatóp eile ag an hidrigin, mar atá, an deoitéiriam agus an tritiam. Tá prótón amháin agus neodrón amháin ag an deoitéiriam, agus tá prótón amháin agus dhá neodrón ag an tritiam. Comhdhéanann deoitéiriam 0.015% den hidrigin nádúrtha. Iseatóp radaighníomhach is ea an tritiam, agus é an-annamh le fáil sa dúlra. Nuair a thagann meath radaighníomhach air, astaíonn sé béite-cháithnín (leictreon) agus é ag déanamh héiliam (³He, an t-iseatóp is éadroime den héiliam atá ar fáil sa dúlra). Tá an tritiam dhá bhliain déag agus thart ar cheithre mí ar leathré.

Fionnachtain[cuir in eagar | athraigh foinse]
An chéad duine a d'aonraigh gás hidrigine agus a thug cur síos foirmeálta ar a shaintréithe, b'é Theophrastus Bombastus von Hohenheim nó Paracelsus é, agus é ar dhuine de cheannródaithe na ceimice. Mheasc sé miotail trí aigéid láidre, ionas gur saoradh gás so-adhainte, ach níor thuig sé go fóill gur dúil cheimiceach a bhí i gceist leis an ngás. Sa bhliain 1671, d'athfhionn Roibeard Ó Baoighill an dóigh seo le hidrigin a tháirgiú, nuair a chuir sé bruscar iarainn trí aigéad báite. Sa bhliain 1766, arís, fuair Henry Cavendish tuiscint nua ar nádúr an gháis mar shubstaint ar leith, go háirithe nuair a thug sé faoi ndeara go ndéanann an gás uisce nuair a dhóitear é. Tháinig sé trasna ar an ngás nuair a bhí sé ag baint trialacha as aigéid agus as airgead beo (mearcair). Shíl sé gur comhchuid shaortha de chuid an airgid bheo a bhí ann, ach cé go raibh an méid seo mícheart ar fad aige, bhí sé in ann cur síos cruinn a thabhairt ar phríomh-shaintréithe na hidrigine, go háirithe go n-iompaíonn sí ina huisce nuair a chuirtear trí thine í. Sa bhliain 1783, bhaist Antoine Laurent Lavoisier a hainm ar an dúil seo, agus dhearbhaigh seisean agus Laplace gur dual don hidrigin uisce glan a dhéanamh agus é ag imoibriú leis an ocsaigin.
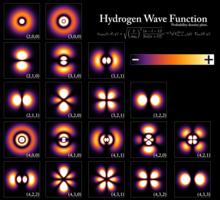
An hidrigin i stair theoiric an chandaim[cuir in eagar | athraigh foinse]
Tá adamh na hidrigine as pabhar simplí ó thaobh an struchtúir de, nó níl ann ach prótón amháin agus leictreon amháin. Mar sin, bhí an-tábhacht leis an hidrigin, chomh maith le speictream an tsolais a astaíonn adamh na hidrigine nó a ionsúnn sé, i bhforbairt na teoirice i leith dhéanamh an adaimh.
Thairis sin, ós rud é go bhfuil móilín na hidrigine agus an caitian a fhreagraíonn dó, mar atá, H2+, iontach simplí freisin, chuidigh sé leis na saineolaithe tuiscint ní ba doimhne a fháil ar nádúr an naisc cheimicigh, go gairid i ndiaidh na tuisceana candam-mheicniúla ar adamh na hidrigine a forbraíodh faoi lár na bhfichidí.
Ceann de na chéad iarmhairtí candam-bhunaithe ar chuir na saineolaithe sonrú iontu, b'é an breathnú a rinne Maxwell leathchéad bliain roimh lá na teoirice iomláine candam-mheicniúla, ná go gcuireann saintoilleadh teasa na hidrigine i gcuimhne iompraíocht na ngás aonadamhach faoi theocht an tseomra, cé go bhfuil an gás hidrigine comhdhéanta as móilíní dé-adamhacha. De réir theoiric an chandaim, is é is cúis leis an iompraíocht seo ná go bhfuil leibhéil chandamaithe an fhuinnimh rothlaigh spréite go fairsing, toisc go bhfuil an móilín féin chomh héadrom.

An Hidrigin sa Dúlra[cuir in eagar | athraigh foinse]
Is í an hidrigin an dúil is coitianta san ollchruinne, nó is adaimh hidrigine iad naoi gcinn as gach deich n-adamh dá bhfuil ann. Tá flúirse hidrigine le fáil sna réaltaí agus sna gásfhathaigh - is é sin, i bpláinéid atá cosúil le hIúpatar agus Satarn. Fáisctear na réaltaí féin as néalta móilíneacha, is é sin, néalta hidrigine atá chomh tiubh is gur féidir do na hadaimh hidrigine iontu teacht le chéile ina móilíní dé-adamhacha (H2). Is í an hidrigin breosla na réaltaí freisin, agus í ag fuinnmhiú an imoibriúcháin chomhleá istigh sa réalta.
An chuid is mó den hidrigin san ollchruinne, is hidrigin aonadamhach í i staid an phlasma. Mar sin, tá sí thar a bheith difriúil leis an hidrigin dhé-adamhach ghásaithe arbh í gnáthstaid na hidrigine aonraithe í ar an Domhan. Nuair atá an hidrigin ina plasma, níl an leictreon agus an prótón ceangailte dá chéile, rud a fhágann go bhfuil an hidrigin in ann leictreachas a sheoladh go réidh agus speictream leanúnach solais a astú - is é sin, tá an cineál seo hidrigine ag luisniú ag gach tonnfhad solais nó ag gach minicíocht solais. Sin é an dóigh a gcruthaítear solas na Gréine féin. Na leictreoin agus na prótóin, is cáithníní iad a bhfuil lucht leictreach acu, agus iad ag idirghníomhú leis na réimsí leictreacha agus maighnéadacha. Is sruth plasma í an ghrianghaoth, go bunúsach, agus nuair a bhuaileann sí réimse maighnéadach an Domhain, feictear na saighneáin (aurora borealis, an chaor aduaidh) ag lasadh suas sa spéir.

Faoi ghnáthbhrú an atmaisféir agus leis an ngnáth-theocht, is í an staid is dual don hidrigin ar an Domhan ná an staid ghásaithe, dhé-adamhach - H2(g). Níl mórán den ghás seo in atmaisféar an Domhain, ós rud é go bhfuil sé chomh héadrom agus nach féidir le himtharraingt ár bpláinéid é a choinneáil ó éalú. Thairis sin, tá an-chlaonadh inti imoibriú leis an ocsaigin, ionas go gcruthaítear uisce. An chuid is mó den hidrigin atá ann ar dhroim an domhain, tá sí ceangailte i gcomhdhúile ceimiceacha, ar nós an uisce féin. Tógann sé cuid mhór fuinnimh na comhdhúile seo a leictrealú agus an hidrigin a aonrú.
Adamh na Hidrigine[cuir in eagar | athraigh foinse]
Is féidir leibhéil fhuinnimh an adaimh hidrigine a oibriú amach sách cruinn de réir shamhail Bohr den adamh, is é sin, an tsamhail ina nglactar leis go bhfuil an leictreon ag timpeallú an núicléis ar an dóigh chéanna a bhfuil na pláinéid ag timpeallú na Gréine. Ní hionann an dá chás go hiomlán, áfach. Is í an imtharraingt an cineál fórsa a choinníonn na pláinéid ó éalú, ach is é an t-aomadh leictreamaighnéadach atá ag gníomhú idir an núicléas agus an leictreon. Deir meicníocht an chandaim go bhfuil an fuinneamh dealaithe ina phaicéid bheaga - ina chandaim - rud a chiallaíonn, sa tsamhail seo den adamh, nach féidir leis an leictreon an núicléas a thimpeallú ach ag fithisí áirithe, agus fad áirithe idir an leictreon agus an núicléas. Má théimid i dtuilleamaí na samhlach candam-mheicniúla den adamh, beidh muid ag baint úsáid as tonnchothromóid Schrödinger. Is é an rud atá ann ná cothromóid dhifreálach(cothromóid nach féidir a fhuascailt gan dul i muinín an chalcalais) a thugann dlús dóchúlachta an leictreoin timpeall an núicléis. Cáilíocht is ea an dlús dóchúlachta a thaispeánann cé chomh dóchúil atá sé an leictreon a fháil i bpointe áirithe i dtimpeallacht a núicléis. Má chaitear leis an leictreon mar seo, - is é sin, mar a bheadh tonn dhamhnach ann -, gheofar torthaí matamaiticiúla atá ag teacht leis na luachanna tomhaiste, níos cruinne ná na luachanna a thugann samhail Bohr den adamh.
Ceimic na hidrigine[cuir in eagar | athraigh foinse]
Níl ach dhá uimhir ocsaídiúcháin ag an hidrigin: +I agus -I. Tá an gás hidrigine iontach so-adhainte, agus é measctha tríd an aer. Nuair a chuirtear hidrigin trí thine, faightear uisce, is é sin, ocsaíd na hidrigine (H₂O). Tá bladhairí na hidrigine beagnach dofheicthe, rud a chiallaíonn nach bhfuil sé éasca dóiteán hidrigine a aithint.
Is féidir leis an hidrigin dul i gcomhdhúile leis na miotail alcaileacha, ionas go ndí-ocsaídeofar go hian hidríde í, H-. Tugtar hidrídí ar na comhdhúile seo. Tá an t-ian hidríde an-éagobhsaí, áfach, agus mar sin, ní féidir na hidrídí seo a thuaslagan san uisce, ó imoibreoidh an t-ian leis an uisce, agus é níos bunata ná na móilíní uisce. Mar shampla, má fhéachtar le hidríd an photaisiam, KH, a mheascadh trí uisce, rachaidh sí ag imoibriú leis an uisce, ionas go n-aonrófar an hidrigin i bhfoirm dúile:
2 KH + 2 H2O -> H2 + 2 OH- + 2 K+
